この講義の内容は下記のYouTubeサイト(再生リスト:生命科学を専攻する学生の為の分子生物学講義)で
動画として視聴できます
https://youtu.be/D5n2LnLEg5U
1. この動画は以下の内容について解説をしています
- ウイルス粒子の基本構造
2. ウイルスの増殖方法とゲノムに基づいた7分類
3. DNAウイルス感染による発癌:パピローマウイルス(HPV)感染による子宮頸がんの発症
4. RNA dependent RNA polymeraseにより増幅するウイルスの感染と発症:コロナウイルスの場合
5. レトロウイルスの感染と発症:エイズウイルス (HIV)感染による後天性免疫不全症候群の発症
6. ガン遺伝子をゲノム内に持つレトロウイルス:Rous sarcoma virus感染による肉腫発症のメカニズム
Key words: キャプシド, エンベロープ, エンドサイトーシス, プラス鎖, マイナス鎖, RNA dependent RNA polymerase, Reverse transcriptase, 逆転写酵素, ファージ,bacteriophage, 子宮頸がん, HPV, コロナウイルス,corona virus, SARS, covid-19, ゲノム複製時のエラー率,スパイクタンパク,MERS, 風邪,コウモリ,自然宿主,ACE2 receptor, 肺胞上皮細胞,突然変異の表記方法,remdesivir, レムデシビル,HIV, エイズウイルス, 後天性免疫不全症候群,潜伏期,LTR, long terminal repeat, CD4レセプター, gag, pol, env, プロウイルス,provirus, リンパ球,カンジダ症,ガン遺伝子, oncogene, v-src, c-src, プロト癌遺伝子
ウイルス粒子の基本構造と分類
2. 様々なウイルスの外観

ここに、様々なウイルスの外観を示しました。このように、ウイルスの外観というのは、様々ですね。まず大きさについてですが、私達、真核生物の細胞はおよそ10μm、細菌が1μm程度、それに対してウイルスの大きさは20から300ナノメーターぐらいです。300ナノメーターは0.3マイクロメーターに相当します。光学顕微鏡で見える限界が200ナノメーターですので、多くのウイルスは光学顕微鏡では見ることができません。電子顕微鏡が必要になります。
3. ウイルス粒子の基本構造
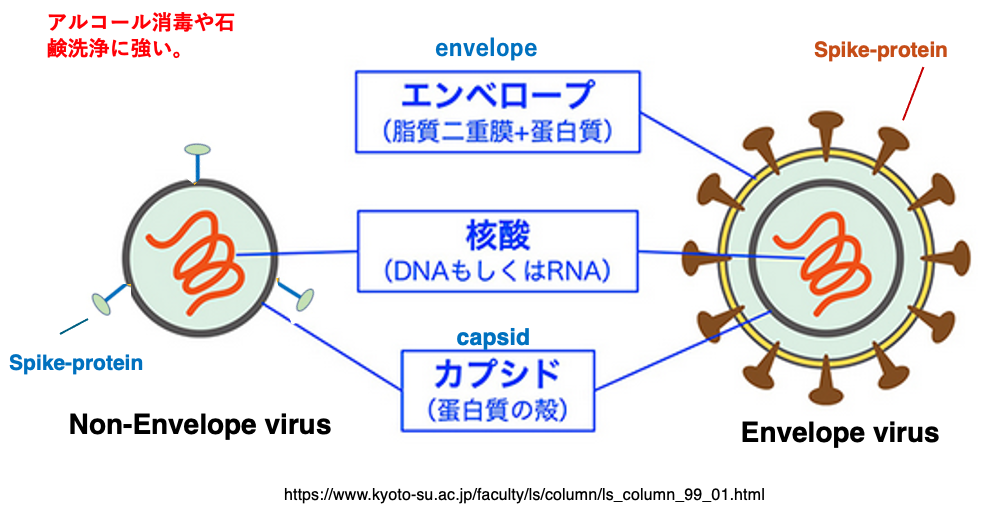
「ここに、ウイルスの基本構造を示しています。まずウイルスは大きく二つに分類されます。一番外側に脂質二重膜で構成されているenvelope 構造を持つenvelope virusと、エンベロープを持たないnon-envelope virusです。エンベロープを持つウイルスでは、その脂質二重膜にいろいろなタンパクが埋め込まれています。
その中で最も重要なのは、スパイクタンパクと呼ばれるたんぱくです。ウイルスは、このスパイクタンパクを使って、宿主の細胞と特異的な吸着を成し遂げます。エンベロープの内側にあるのが、キャンプシドと呼ばれるタンパク質の殻です。non-envelope virusの場合は、キャンプシドを構成するタンパクの殻が最外層ということになります。non-envelope virusの場合には,そこにスパイクタンパクが埋め込まれています。キャッシュの殻の中に核酸,すなわちDNAもしくはRNAがゲノムとして含まれています。
エンベロープは脂質二重膜なので、アルコールや石鹸により,簡単に破壊されてしまいます。一方,キャプシドはタンパクの殻なので、アルコールや洗剤にある程度の耐性を示します。従って、non-envelope virusの方が、アルコール消毒や石鹸によって不活性化することが難しいということになります。
4. Capsidタンパクが形成するウイルスの外観
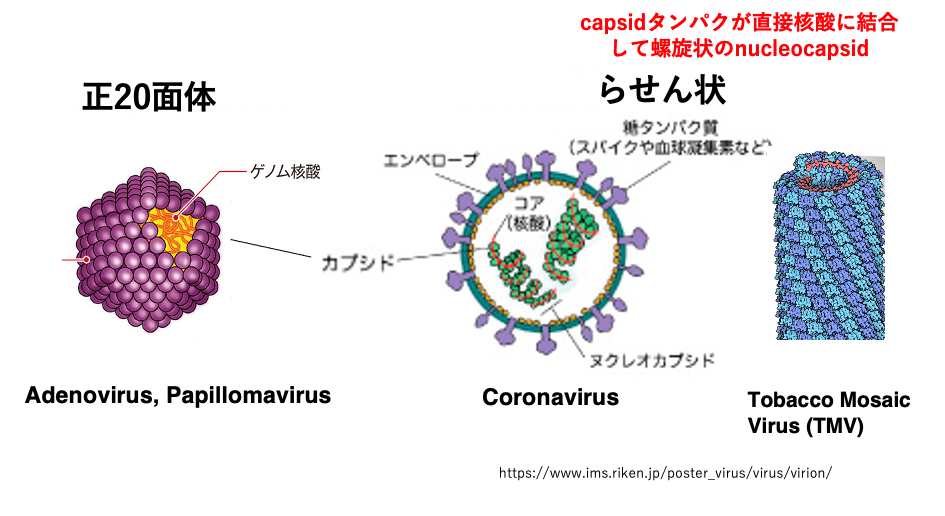
キャプシドタンパクが形成する殻の外観について見ていきます。キャプシドタンパクは、正20面体、あるいはらせん状の立体構造を形成します。正20面体のキャプシドは,小さなタンパクが規則正しく集合することで形成されます。その中にゲノム核酸が収納されています。
このような,キャプシドを持つウイルスとしては,アデノウイルスやPapillomavirusがあります。一方、ゲノムDNAまたはRNAにキャプシドタンパクが直接付着することで、らせん状のヌクレオキャプシド、すなわち核酸とキャプシドタンパクの複合体が形成されます。
核酸にタンパクが付着することで、らせん状のキャプシドが出現します。このような例としては、コロナウイルスあるいはタバコモザイクウイルスがあります
5. エンベロープを持つウイルスの宿主細胞への初期感染過程
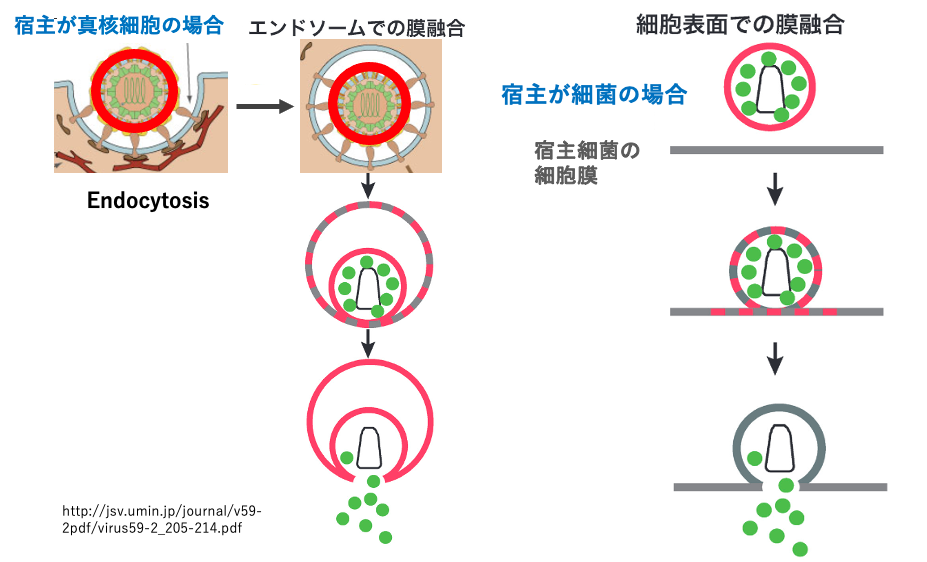
エンベロープを持つウイルスの宿主細胞への初期感染の過程を見ていきます。まず、宿主細胞が真核生物の場合ですが、ウイルスはスパイクを用いて、その表面に特異的に吸着します。ウイルス粒子はエンドサイトーシスにより細胞中に侵入していきます。
その次に,細胞質の中で、ホスト細胞の脂質二重膜とエンベロープの膜が融合することによって、キャプシドが細胞質内に放出されます。一方、ウイルスの宿主が細菌の場合は、エンベロープが細菌の細胞質膜と融合することにより,キャプシドが直接,細胞質の中に放出されます。
6. non-envelope virusの細胞内への侵入
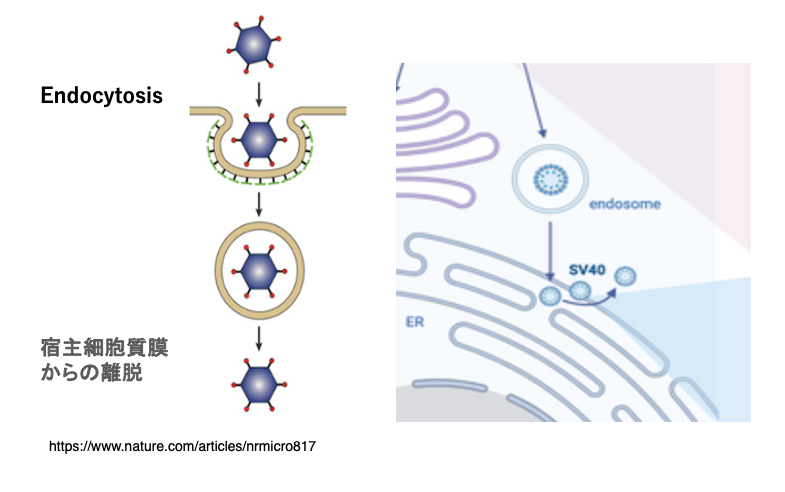
次にnon-envelope virusの細胞内への侵入について解説をしていきます。non-envelope virus場合、capsidが最外層ということになります。宿主表面に付着したcapsidは、endocytosisによって細胞質の中に侵入します。
細胞質の中では、宿主の細胞質膜からできている膜が最外層ということになります。この膜から、どのようにしてウイルス粒子が放出されるのかについては、幾通りかの方法があります。
例えば、SV40の場合、endocytosis membraneが、ER membraneと融合することによって、ウイルス粒子が細胞質内に放出されます。
7. ウイルスの分類

ウイルスの分類についてです。ウイルスの粒子内にある核酸、それがDNAなのか、RNAなのかと,ウイルスゲノムがどのようにして複製されるかによってウイルスは7つに分類されます。
8. DNA鎖,RNA鎖につけられる名称
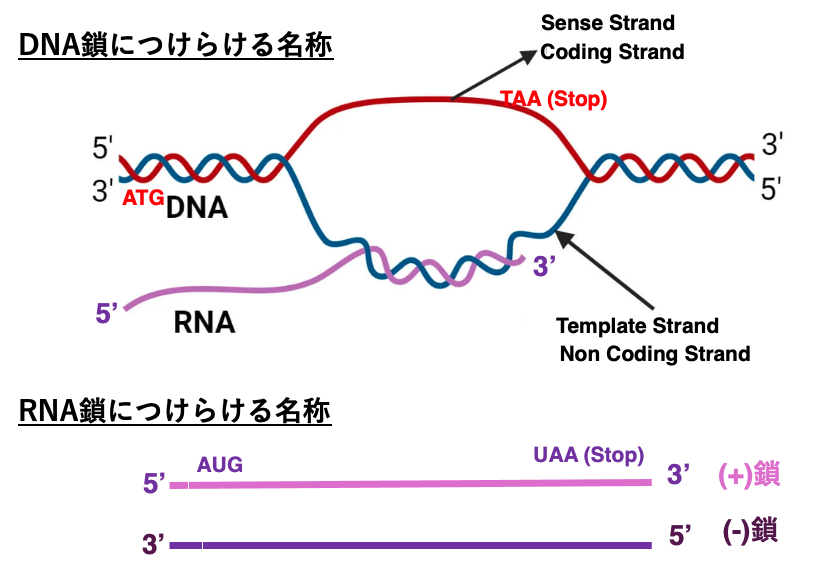
DNAの鎖、あるいはRNAの鎖には様々な名称が付けられていますのでそれについて、復習をしておきます。
まず、この青色のDNAの鎖ですが、この鎖は、転写の鋳型として働いていますので、template strandと呼ばれます。このtemplate strandが転写されて生成されたメッセンジャーRNAの塩基配列と、赤色のDNA鎖の塩基配列はよく似ています。ウラシルとチミンの違いだけです。そのため赤いDNAの鎖は、coding strand、あるいはsense strandと呼ばれます。一方、この赤い鎖がcoding strandとランドと呼ばれることから、青色のDNA鎖は、non-coding strandとも呼ばれます。
一方こちらは、RNA鎖につけられる名称を示しています。これは通常のメッセンジャーRNAですね。翻訳開始コドンであるAUGとUAA終始ドンを持っています。このように、アミノ酸配列の情報を持つmRNAの鎖はプラス鎖というふうに呼ばれます。それに対して、このプラス鎖と相補な配列を持つRNA鎖は、マイナス鎖と呼ばれます。
9. RNAをウイルス粒子内にゲノムとして持つRNAウイルスの4分類
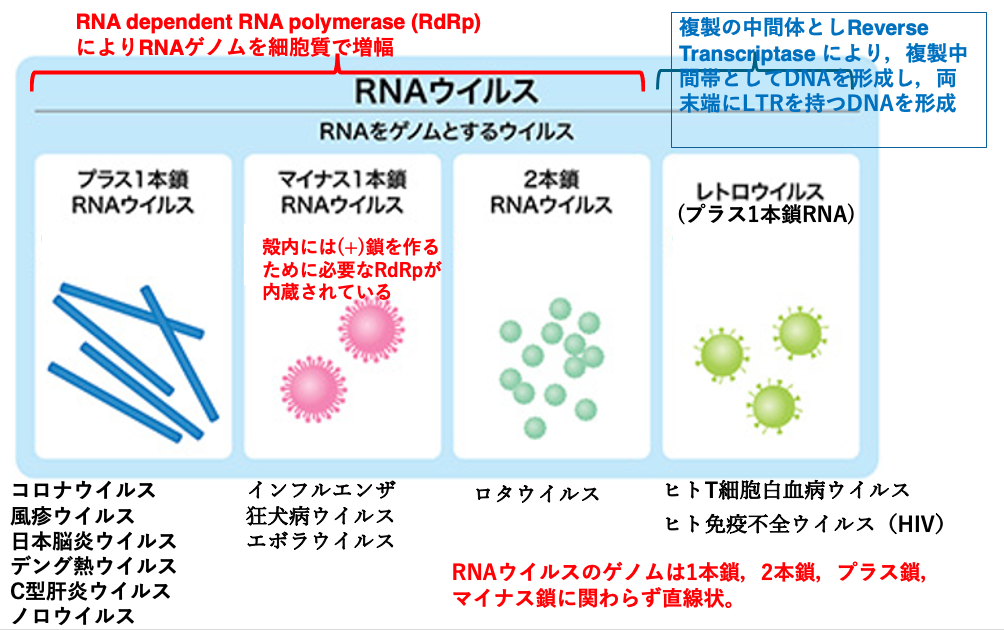
RNAをウイルス粒子内にゲノムとして持つようなウイルスは、RNAウイルスと言われます。RNAウイルスは4種類に分類されています。そのうち、3種類は、RNA dependent RNA polymeraseにより,ゲノムが細胞質の中で増幅されます。
もう1種類は、retro virusと呼ばれていて、複製の中間体としてreverse transcriptaseにより複製中間体としてDNAを形成し、両末端にロングターミナルリピート持つようなDNAを形成して増えます。
RNA dependent RNA polymeraseでRNAゲノムが増幅されるようなウイルスには、マイナス1本鎖を持つようなタイプ,プラス 1本鎖を持つようなタイプ、それから2本鎖RNAを持つタイプがあります。プラス1本鎖RNAを持つ例とすると、コロナウイルスや風疹ウイルスなどがあります。マイナスは1本鎖をゲノムとして持つようなRNAウイルスとしては、インフルエンザウイルスや狂犬病ウイルスがあります。2本鎖RNAをゲノムとして持つようなものとしては、ロタウイルスが知られています。一方、逆転写酵素により、DNA中間体を形成して増えるレトロウイルスには、ヒトT細胞白血病ウイルスやヒト免疫不全ウイルスなどがあります。
10. DNAウイルスの3分類
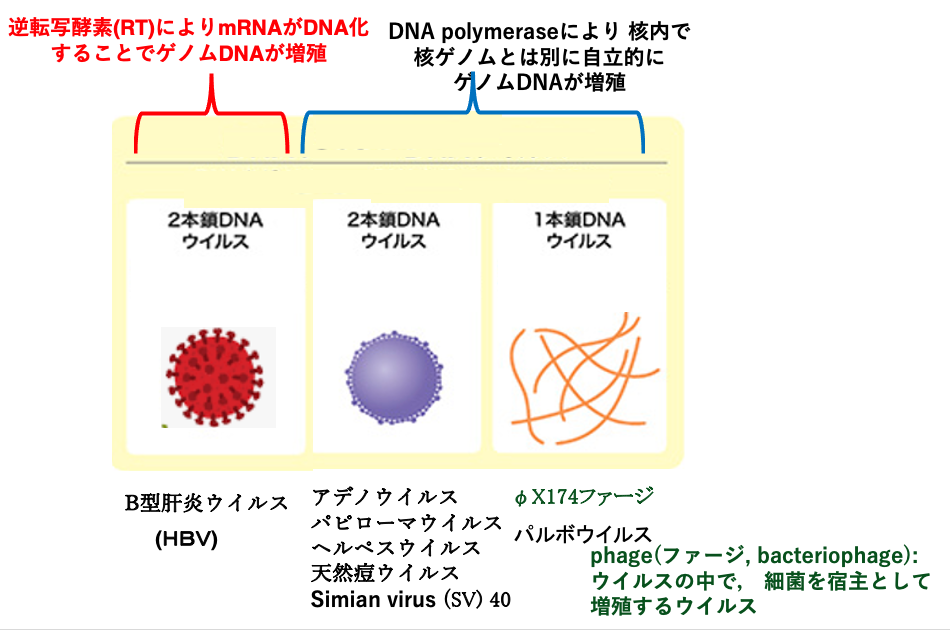
DNAゲームをウイルスの粒子内に持つものは、DNAウイルスと呼ばれますが、それは3つに分類されます。まずDNA polymeraseにより、核内で宿主のゲノムとは独立して自己のゲノムを増幅させるDNAウイルスを2つの群に分類します。
一つ目の群は、2本鎖DNAをゲームとして持っているウイルスです。アデノウイルスや天然痘ウイルス,SP40などが,この群に含まれます。もう一つは、ゲノムとして1本鎖DNAを持っているウイルスの群です。φX174 phageがこの群に含まれます。
phageという言葉が出てきましたので、ここで少し説明を加えておきます。phageあるいはbacteriophageと呼ばれるものは、ウイルスの中でも細菌を宿主として増殖するウイルスを指します。真核生物の細胞を宿主として増えるものは、phageとは呼ばれません。3つ目のウイルス群は、2本鎖DNAをゲノムとして持つが、逆転写酵素によりメッセンジャーRNAをDNA化することでゲームの増幅を果たすようなDNAウイルス群です。B型肝炎ウイルスは,このようなウイルスの一種です。このように、DNSウイルスは三つに分類されています。
11. ゲノムDNA形状によるDNAウイルスを分類

ゲノムDNAの形状によってDNAウイルスを分類するとこの表のように分類することができます。環状の1本鎖である例としては,φX1748 phageなどがあります。環状の2本鎖ゲノムを持つ例としれは、SP40やポリオウイルスがあります。これらの環状DNAウイルスは宿主の核内でori配列から、DNAポリメラーゼによって複製されます。
また、直鎖状の1本鎖DNAをゲノムとして持つ例としと、パルボウイルスがあります。直鎖状2本鎖ゲームとして持つDNAウイルスとすると、T4 phage, アデノウイルスやヘルペスウイルスがあります。それらの直鎖状ゲノムの多くは環状化して、核内で宿主のDNAポリメラーゼによって複製されます。
12. パピローマDNAウイルスの感染による子宮頸がんの発症
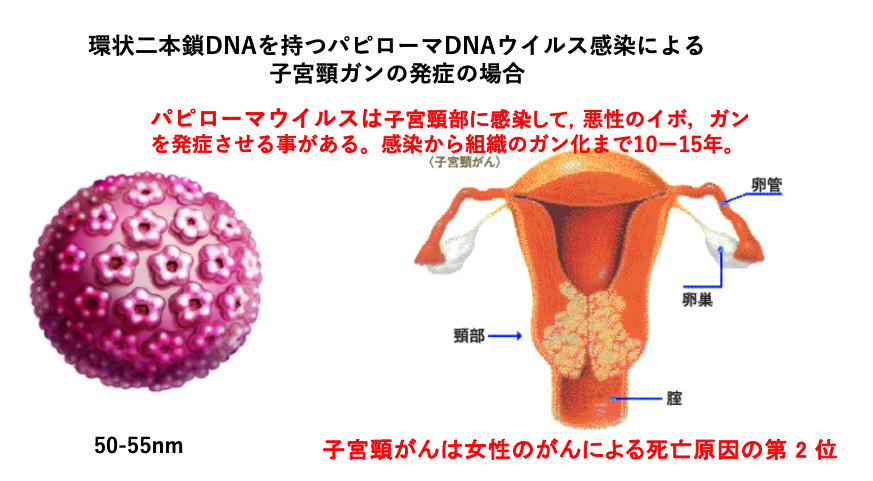
これからいろいろなウイルスの感染による発癌について解説をしていきたいと思います。まずは、DNAウイルスの感染による発癌について説明をします。例として、環状2本鎖DNAを持つパピローマDNAウイルスの感染による子宮頸がんの発症について説明をしていきます。パピローマウイルスは、子宮頸部に感染して、悪性のイボを発症させることがあります。それが,長い年月をかけてガン化すると考えられています。ウイルスの感染から癌化するまでには非常に長い時間を要し、10年から15年を要すると言われています。この子宮頸癌は、女性の癌による死亡率の現在第2になっています。パピローマウイルスの大きさは、直径が50から55ナノメーターぐらいです。
13. パピローマウイルスにコードされている遺伝子
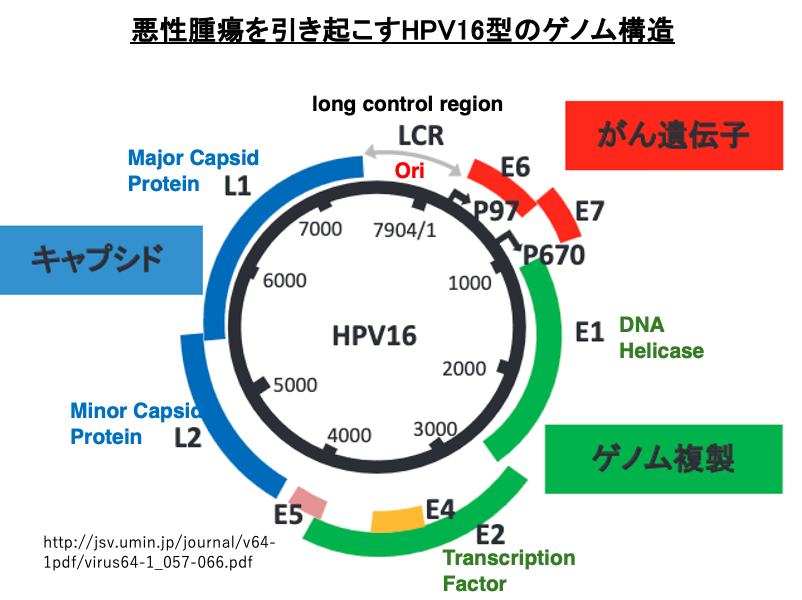
悪性の子宮頸癌を引き起こす。人パピローマウイルスの16型のゲノムについて説明をします。パピローマウイルスは、環状の2本鎖DNAをゲノムとしています。タンパクコーディング領域は全て一つの鎖の上に配置されています。
そのゲノムにコーディングされている遺伝子として、ウイルスのキャプシドタンパク質をコードしているL1とはL2があります。また、ゲノム複製に関わる遺伝子として、E1とE2遺伝子があります。E1遺伝子はDNA helicase、E2はtranscription factorをコードしています。
また、癌を引き起こすのに関わる遺伝子として、E6とE7遺伝子が知られています。ここには、DNA複製に関わるori sequenceがコードされています。
14. パピローマウイルスの感染経過
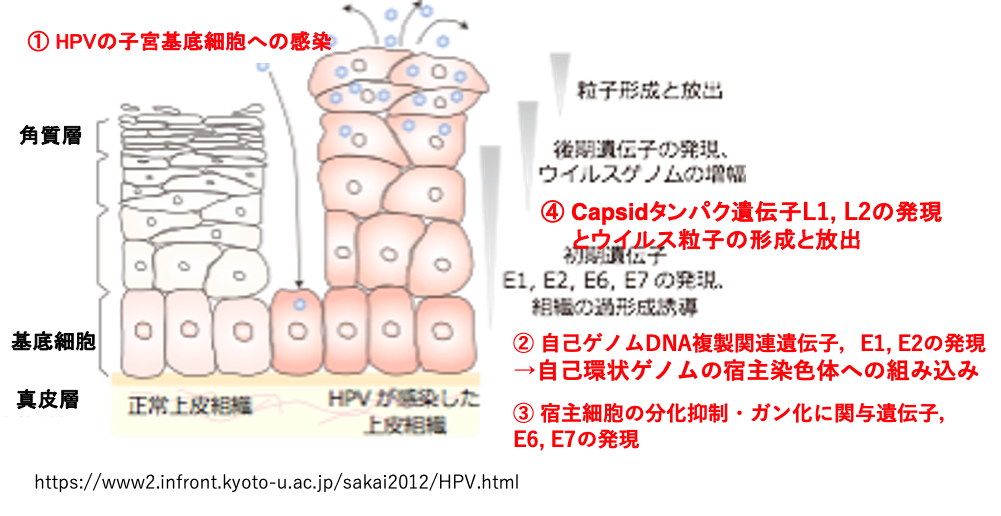
人パピローマウイルスは小さな傷などを通じて、まず,真皮層の上,角質層の下にある基底細胞に感染をします。感染が成立すると自己ゲノムのDNA複製に関連する遺伝子E1とE2を発現させます。それにより、自己の環状ゲームの数を増やし,やがて環状ゲームを宿主染色体へ組み込んでいきます。
続いて、宿主細胞の分化抑制や癌化に関与するような遺伝子E6とE7を発現していきます。このような遺伝子の発現にも関わらず、基底細胞が時間を経て,細胞分裂をしない角質層に変化していきますと,ウイルスは自己の粒子形成に必須なキャプシドタンパク遺伝子であるL1,L2を発現させて、宿主の細胞内でウイルス粒子内で形成し、ウイルス粒子を周辺細胞に放出します。放出されたウイルスはまた傷などを通して基底細胞に再度感染していくことになります。このようなサイクルを繰り返すうちに,ガン化した基底細胞が生じることがあります。
15. パピローマウイルスによる細胞のがん化
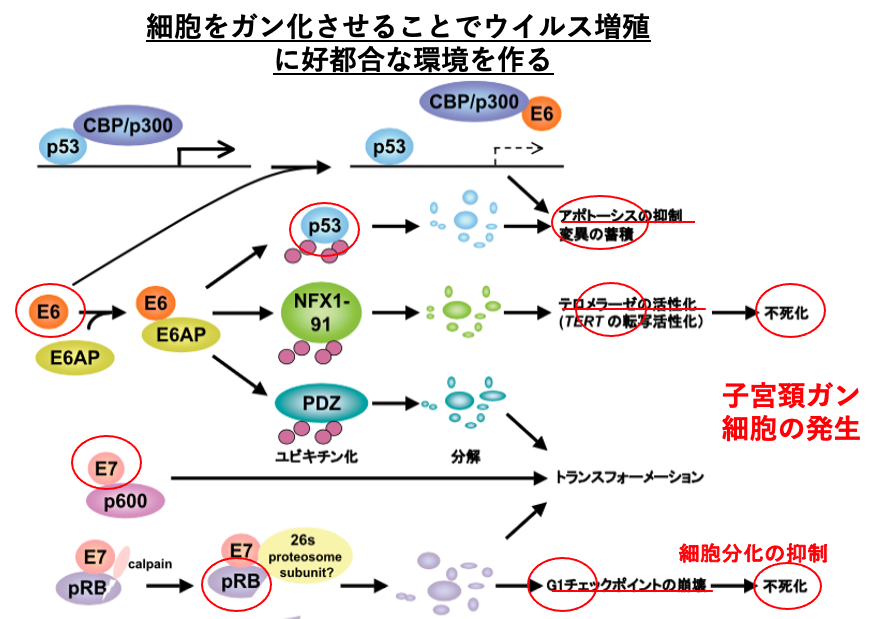
パピローマウイルスによる細胞のがん化について、もう少し詳しく解説をしていきます。このウイルスはガン化に関与する遺伝子として、E6遺伝子をそのゲーム内に持っています。E6タンパクは、p56などに働きかけて、その働きを抑制することによって、アポトーシスの抑制、変異の蓄積を促していきます。同時にテロメラーゼを活性化させて、細胞を不死化させます。
もう一つのガン化遺伝子としてE7遺伝子があります。E7タンパクはPRBタンパクに付着して、宿主のゲノム複製のG1チェックポイントを崩壊させます。そのことにより、細胞分化の抑制と不死化を促します。このようなE6およびE7遺伝子の働きを通じて、自分が感染した子宮頸部の細胞をがん化させます。こういうふうに、細胞がん化させることで、ウイルス自身は活発に増殖できる環境を作りだしていると思われます。
RNA dependent RNA polymeraseにより増幅するRNAウイルス感染による発症
コロナウイルス(covid-19)感染による急性呼吸器症候群(SARS)の発症
次にRNA dependent RNA polymeraseにより増幅するようなRNAウイルスの感染と発症について解説をしていきます。その例としてここでは、コロナウイルス, covid-19, の感染によるsevere acute respiratory syndrome、いわゆるSARSの発症について解説をしていきます。
16. RNA dependent RNAp0lymeraseによるウイルスゲノムの増幅
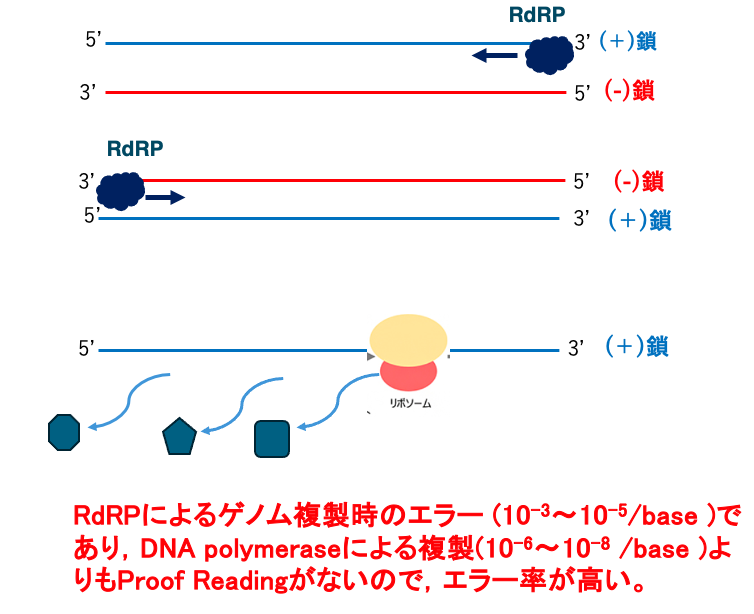
RNA dependent RNAp0lymeraseによるウイルスゲノムの増幅について説明をしていきます。例えば、このウイルスの場合、ウイルス粒子に入っているのはプラス鎖のRNAです。プラス鎖の意味については既に説明をしましたが、この鎖がリポソームによって翻訳されることによって、タンパクが作られる。そのための情報を持っているようなRNA鎖である事を意味しています。
このプラス鎖を持つようなRNAの鎖を鋳型としてRNA dependent RNAポリメラーゼにより、新しい鎖が合成されますと、出来た鎖はプラス鎖に対して相補的な塩基配列を持つ,マイナス鎖となります。 一方、このウイルスの場合、粒子に入っているのがマイナス鎖であるとすれば、RNA dependent RNAポリメラーゼ作られたRNA鎖はプラスさということになります。
RNA dependent RNAポリメラーゼによる複製時のエラーは,塩基当たり10のマイナス3乗から10のマイナス5乗であると言われています。これはDNAポリメラーゼによる複製が、塩基あたり10のマイナス6乗から10のマイナス8乗であるということと比較して、およそ1000倍高くなっています。このように、RNA dependent RNAポリメラーゼによる複製のエラー率が高いのは、Proofリーディングの機構がないことによります。
17. コロナウイルスの基本構造
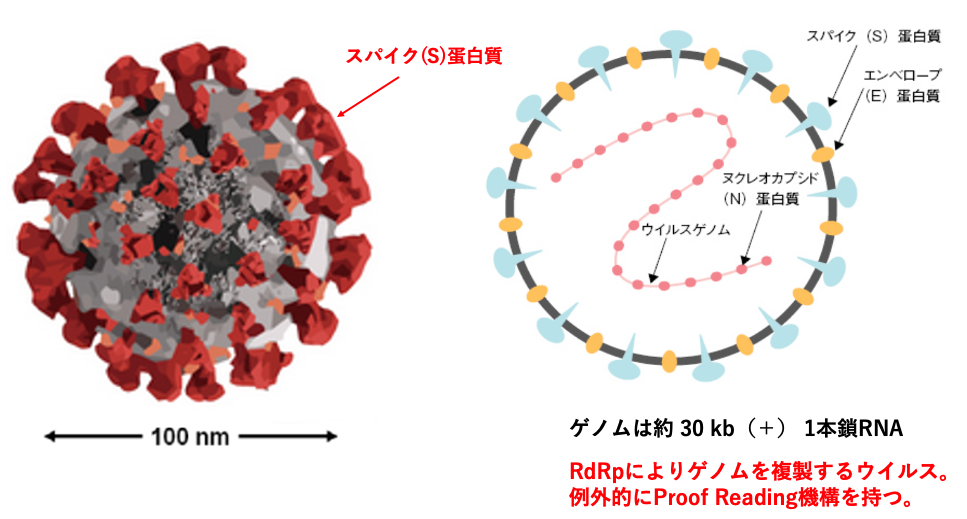
コロナウイルスの基本構造から説明をしていきます。これがコロナウイルスの外観ですけれども、エンベロープに宿主との特異的な吸着に関するスパイクタンパクが埋め込まれています。直径がおよそ100ナノメートルです。その内部構造をここに示しています。
エンベロープにスパイクタンパクとEタンパクが埋め込まれています。キャプシドタンパクは、そのゲノムであるプラス1本RNAに直接付着するタイプです。ゲノムの大きさは約30キロベース、これがコロナウイルスの基本構造です。非常に大きなRNAゲノムを持つウイルスで、RNA dependent RNA polymeraseによって複製されますが、このRNAウイルスは例外的にproof readingの機構を持っています。そのため、非常に大きなゲームであっても、ある程度の精度を複製することができているというふうに考えられます。
18. 詳細なコロナウイルスの構造
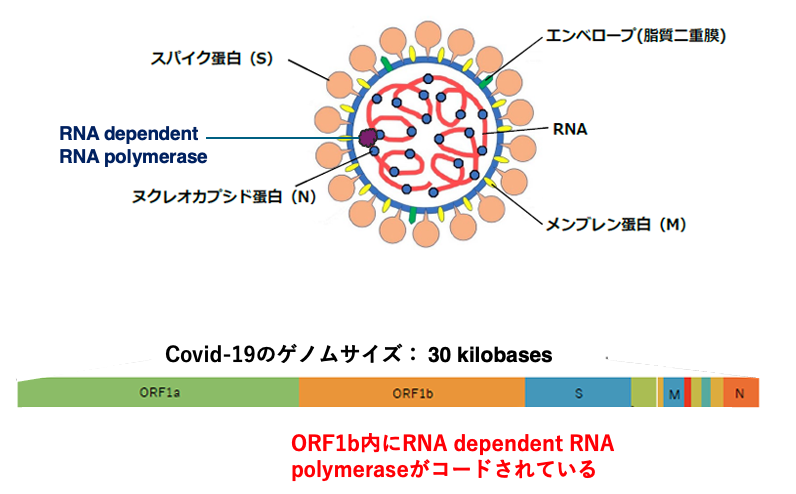
ここにもう少し詳しい,コロナウイルスの構造を示しました。エンベロープには、Sタンパクの他に、NタンパクやMタンパクが埋め込まれています。また、ウイルス粒子には既にRNA dependent RNAポリメラーゼのタンパクが内蔵されています。
これが最近流行したコロナウイルスの一種であるCovid-19のゲノム構造ですが、ORF1Bには、RNA dependent RNAポリメラーゼがコードされています。その他、Sたんぱく、Mタンパク、Nタンパクなどがこのゲノム上にコードされているということがわかります。
19. 様々なコロナウイルスに感染した場合の症状
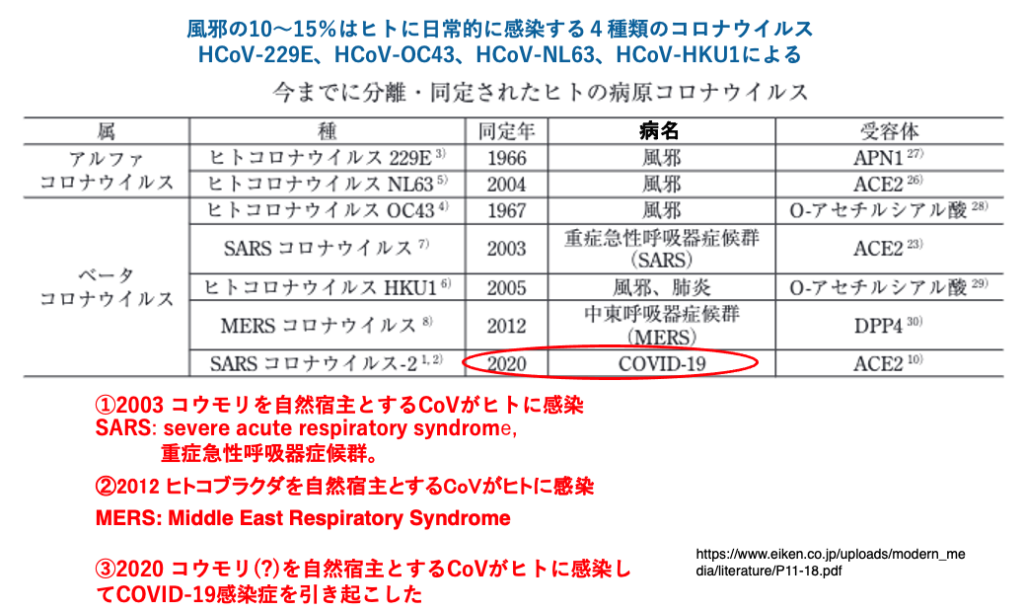
ここでコロナウイルスに感染した場合の症状についてまとめておきたいと思います。私達は普段、いわゆる風邪をひきますね。そういう風邪ひきの10%から10%は、人に日常的に感染する4種類のコロナウイルスが原因であるというふうに言われています。ヒトコロナウイルスの229E。あるいはOC43, NL63, HKU1と言われるような、日常的に人の間で感染を繰り返しているヒトコロナウイルスに感染した場合は、いわゆる風邪の症状を引き起こすことがあります。
一方、2003年には、コウモリを自然宿主とするようなコロナウイルスが人に感染しました。元々が、人が自然宿主でないようなコロナウイルスに感染しますと、非常に重篤な呼吸系の疾患を発症することになります。いわゆるSARSと言われるような病状を発症することになります。
2012年には、ヒトコブラクダを自然宿主とするような、コロナウイルスが人に感染をしました。主として中東地域で流行しましたので、Middle East Respiratory Syndrome, MERSと名付けられました。これも非常に重篤な呼吸器系の疾患を伴う病状が見られました。最近,起こったのが2020年ですね。おそらくは、コウモリを自然宿主とするようなコロナウイルスが人に感染することによって、重篤な呼吸系の疾患を引き起こしました。このように、人以外を自然宿主とするようなコロナウイルスが種の壁を越えて人に感染した場合には、非常に重篤な呼吸系の病状を引き起こすということになります。
20. コロナウイルスのヒト細胞への吸着
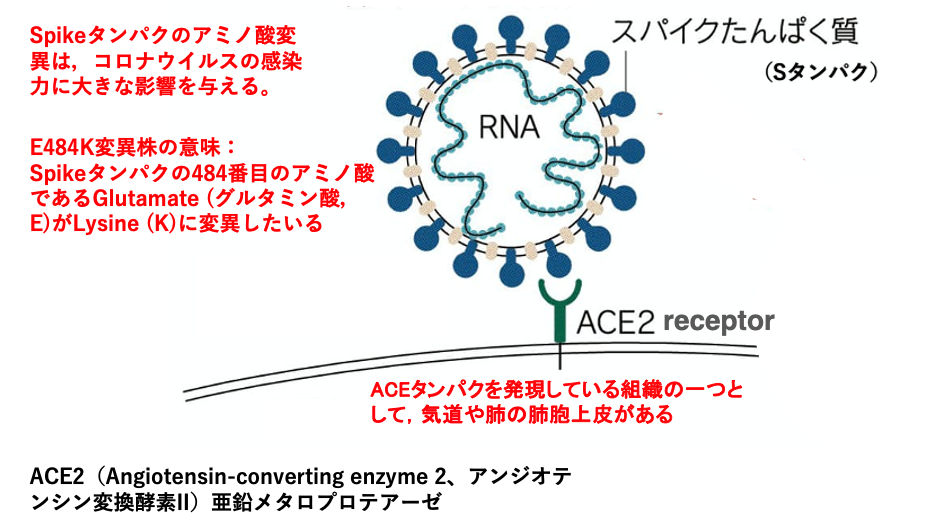
コロナウイルスの感染の最初の反応である細部への吸着について説明をしていきます。コロナウイルスのエンベロープに埋め込まれているスパイクタンパクは、ACEリセプタータンパクと特異的に結合することができます。
ACEリセプタータンパクというのは、メタロプロテアーゼレセプターのことを指します。このリセプターは、気道や肺の肺胞上皮細胞でたくさん発現されています。従ってコロナウイルスは、肺の肺胞上皮細胞に感染していくことになります。スパイクタンパクのアミノ酸変異は、コロナウイルスの感染力に大きな影響を与えます。
このことから、コロナウイルスの変異は、スパイクタンパクのアミノ酸変異に注目して記載されることが多いです。例えばE484K変異株というふうに記載されている場合、その意味するところは、スパイクタンパクの484番目のアミノ酸であるグルタミン酸, Eがリジン,Kに変異している事を示しています。こういう変異がスパイクタンパクに起きているコロナウイルスであるということを意味しています。
21. Corona virusの増殖サイクル
Corona virusの増殖サイクル
Corona virusの増殖サイクル
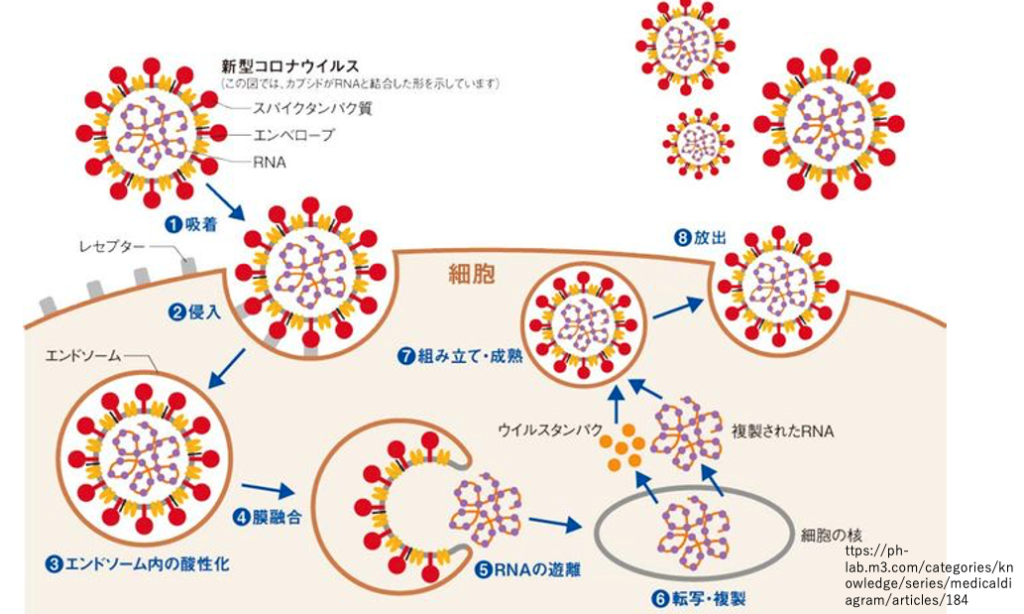
続いて、コロナウイルスの増殖サイクルについて説明をしていきます。コロナウイルスは肺胞上皮細胞に吸着した後、エンドサイトーシスによって細胞質内に飲み込まれていきます。
エンドサイソーム内のpHが酸性化することで、外側のエンドソーム膜と内側のエンベロープ膜が融合して、中からゲノムであるRNAが細胞質内に放出されます。ゲノムRNAは核に移行し、RNA dependent RNAポリメラーゼにより、そのRNAの複製が行われます。RNAは、細胞質内で翻訳されて、ウイルス粒子の構築に必要なタンパクが作られます。
ウイルス粒子タンパクが集合して、エンベロープが形成されますと、その中にゲノムであるRNAは取り組まれ、やがて細胞膜表面から放出されていくということになります。これがコロナウイルスの増殖サイクルです。
22. コロナウイルスの治療薬レムデシビルの作用機序
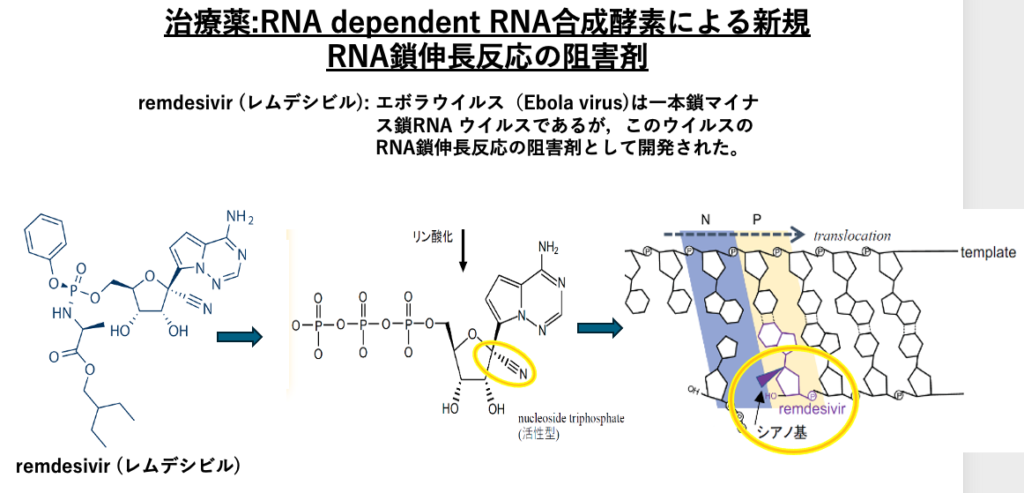
コロナウイルスに感染した場合の治療薬の一つである。レムデシビルについて説明をしておきます。このレムデシビルは、元々,Ebola virusの治療薬として開発されたものです。エボラウイルスは1本鎖でマイナスのRNAをゲームとして持っています。このウイルスにおいて,RNA dependent RNAポリメラーゼによる,相補鎖の伸長反応を阻害する薬剤として開発されたのがレムデシビルです。
ここに,レムデシビルの構造式を示しています。レムデシビルは、細胞内でこのように変化して、ヌクレオチド3リン酸のアナログとなります。この部分にシアノ基があるのが特徴です。このレムデシビルは、RNA dependent RNAポリメラーゼによって取り込まれて、このようになります。レムデシビルこが取り込まれると,この部分にあるシアノ基の立体障害により、RNA dependent RNAポリメラーゼは,次のヌクレオチド3リン酸を取り込み,結合させることができません。このようなメカニズムで,レムデシビルはコロナウイルスの増殖を阻害します。
23. 長い潜伏期をもつレトロウイルスの感染と発病

長い潜伏期を持つレトロウイルスの感染と発病について解説をしていきます。まず、レトロウイルスですけれども、これはゲームとしては、1本鎖プラス鎖のRNAを持っています。しかし、そのゲノムの増幅については、RNA dependent RNAポリメラーゼではなくて、逆転写酵素、reverse transcriptaseが使われます。
また、逆転写により作られたDNAは、long terminal repeatを持ちます。このlong terminal repeatを持つDNAは、宿主ゲノムに埋め込まれるというステップを持ちます。そのようなレトロウイルスの一種に,AIDSウイルスがあります。Human Immunodeficiency Virus, HIVウイルスですね。HIVウイルスの場合、5年から10年の長い無症状期間,潜伏期を経て、白血球数の低下による免疫力の低下を引き起こします。後天性免疫不全症候群を発症します。これにより、肺炎や悪性腫瘍などに罹りやすくなり,死に至る場合があります。
24. HIVウイルスの基本構造
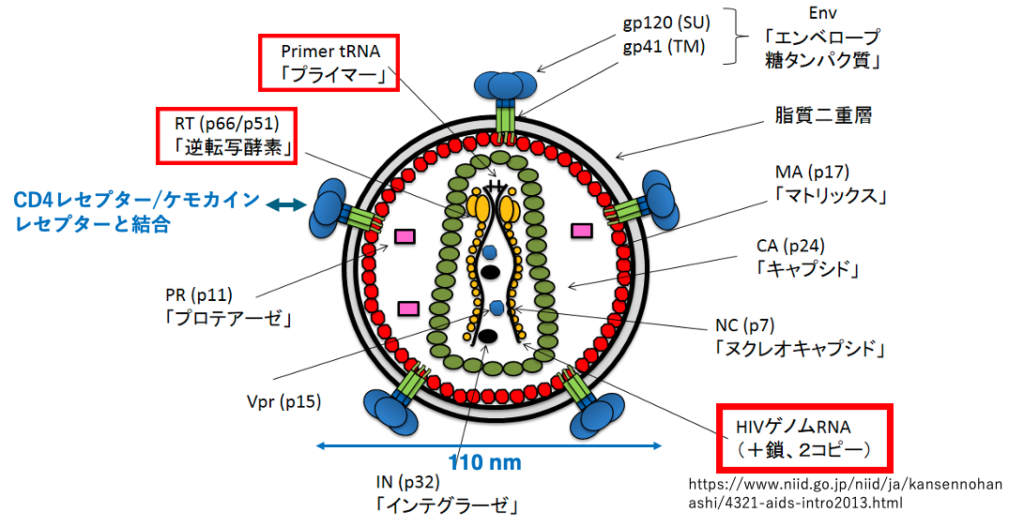
HIVウイルスの基本構造について説明をしていきます。エンベロープがあってそこにスパイクタンパクが埋め込まれています。このスパイクタンパクは、宿主細胞の表面にあるCD4レセプターケモカインレセプターと特異的に結合をします。
ゲノムとすると、プラス鎖の1本鎖RNAですが、それが2コピー含まれています。また、このRNAゲノムを逆転写してDNAにするための逆転写酵素が,予め粒子内に組み込まれています。また逆転写反応に必要なプライマー,そのプライマーとしてtRNAが使われますが、tRNA分子も粒子内に組み込まれています。
この緑色は、キャプシドタンパクを示しています。このようにRNAゲノム,逆転写酵素tRNAプライマーが、キャプシドタンパクの殻の中に含まれています。これがHIVウイルスの基本構造ということになります。大きさは直径でおよそ110 nm程度です。
25. HIVウイルスのゲノム構造
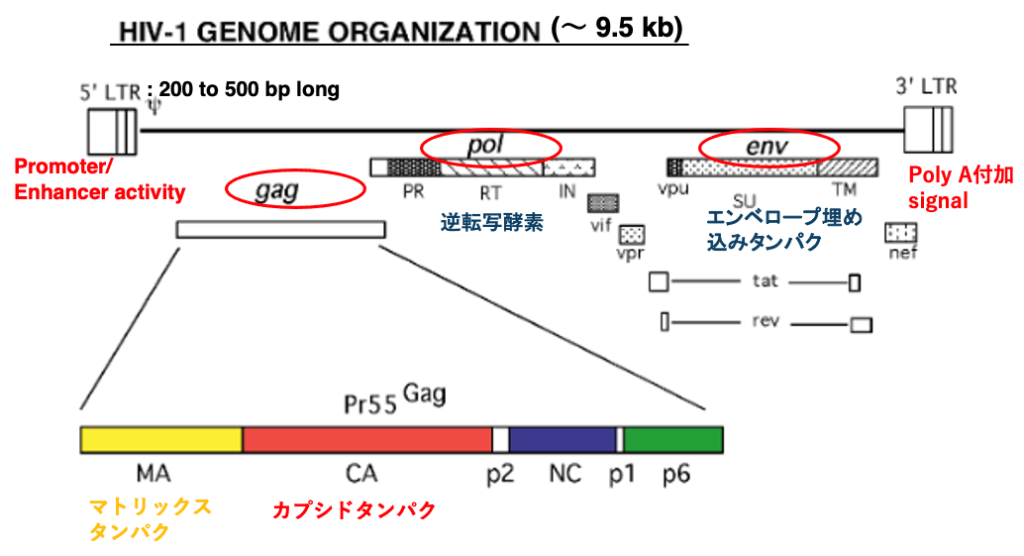
HIVウイルスのゲノム構造について解説をします。ここには、逆転写されたHIVウイルスのゲノム構造を示しています。まず、long terminal repatがあります。5‘末端のlong terminal repatは、プロモーター活性や、enhancer活性を持っています。一方、3‘末端末端のlong terminal repatはポリA付加シグナルを持っています。
また、大きなタンパクコーティング領域としてGAGがあります。GAG領域には、マトリックスタンパクやキャプシドタンパクなどが含まれます。次にPOL領域があります。この領域には、逆転写酵素などがコードされています。最後に、ENV領域があります。この領域にはエンベロープタンパクなどがコードされています。全体として、HIVウイルスは,DNAに逆転写された状態で、およそ9.5キロベースという長さを持っています。
26. HIVウイルスが感染するCD4 receptor positive T cell
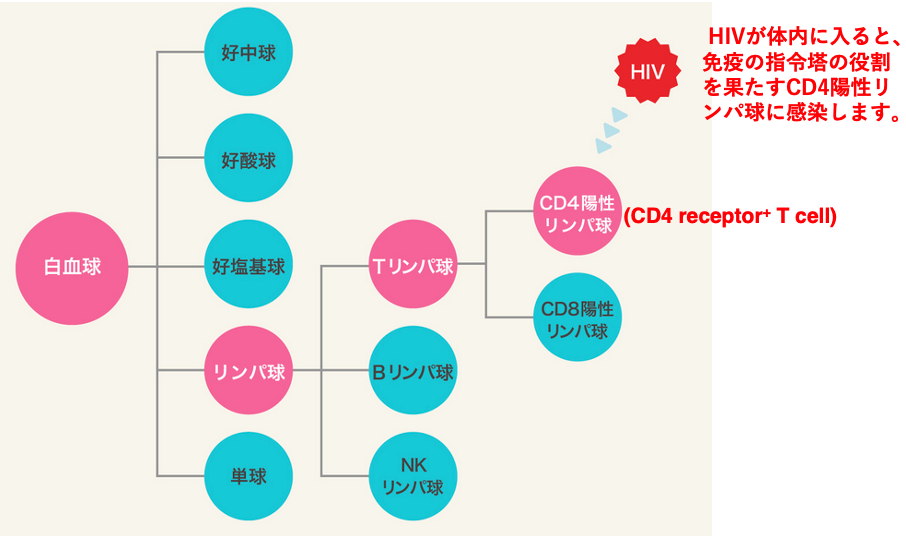
ここには、白血球が分化してできる細胞群を示しています。白血球が分化することにより、いろいろな細胞ができます。
リンパ球はその一つです。リンパ球は更に分化して、Tリンパ球やBリンパ球にわかれます。また,Tリンパ球が分化してできる一つに、CD4 receptorを発現しているCD4 receptor positive T cellがあります。HIVウイルスが感染するのは、このCD4 receptor positive T cell。この細胞は免疫系において中心的な役割を担っています。
27. HIVウイルスの増殖サイクル
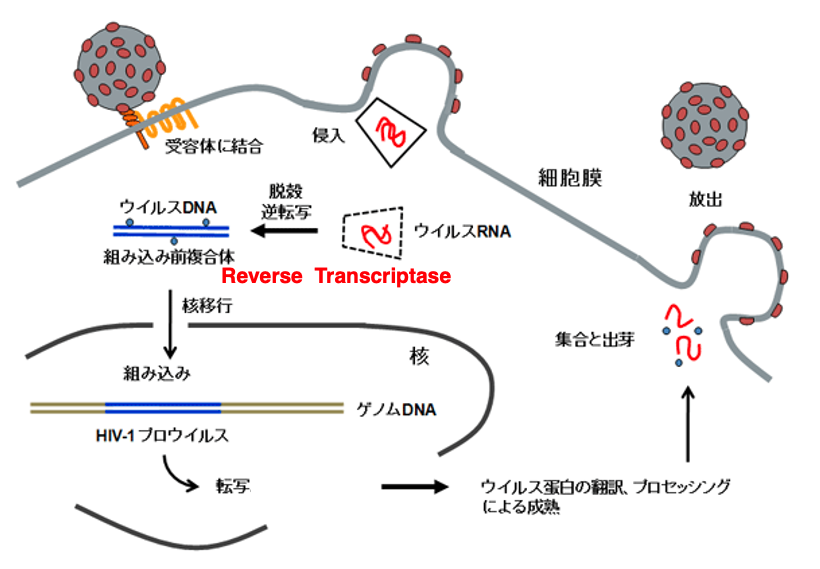
HIVウイルスの増殖サイクルについて説明をします。ウイルスはまず、CD4レセプターに特異的に吸着します。吸着が終わると、ウイルスのエンベロープ膜と、ホストの細胞質膜が融合し、ウイルスからキャプシドの殻が放出されます。キャプシドの殻タンパクはやがて分解され、その中にあったウイルスRNAゲノムが細胞質の中に放出されます。ウイルス自らが持ち込んだ逆転写酵素により、RNAゲノムは、2本鎖DNAに変換されます。
2本鎖DNAは核内に移行し,やがてゲノム内に組み込まれてきます。このように、ウイルスが宿主のゲノム内に組み込まれた状態を、プロウイルスといいます。エイズウイルスの場合、5年から20年という長い間、プロウイルスの状態が続きます。その間は,ウイルス遺伝子の活発な転写が見られません。したがって、病状も顕著ではない潜伏期が続きます。
ホストの体調が変化したことなどをきっかけに、ウイルスの転写が活発化します。ウイルスRNAが翻訳されることによって、ウイルス粒子を再構成するのに必要なタンパクが細胞質内に蓄えられ、それをもとに、多くのウイルス粒子が形成されます。それらは、やがて細胞の表面から放出されていきます。これがHIVウイルスの増殖サイクルです。
28. AIDS発症までのCD4陽性リンパ球数の変化
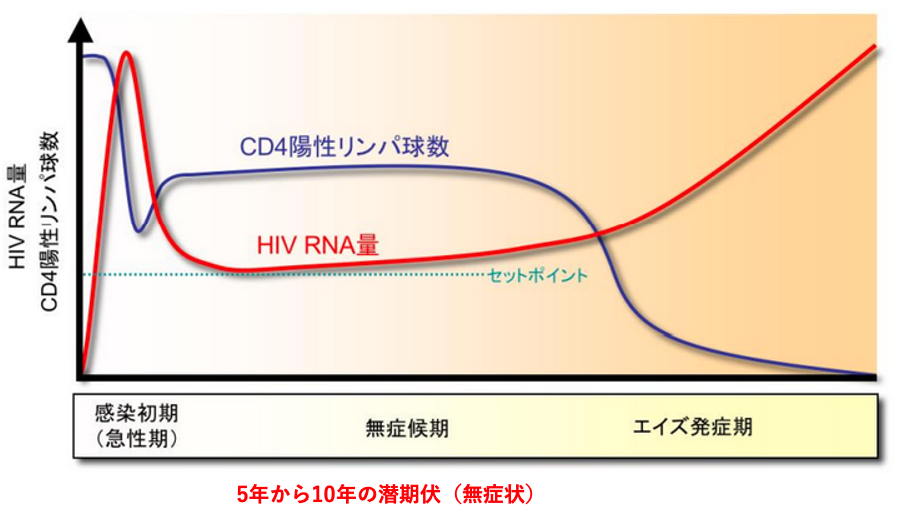
この図は、HIVウイルスの感染からAIDS発症までのCD4陽性リンパ球数の変化をまとめたものです。HIVウイルス感染の直後に一旦CD4陽性リンパ球は減りますが、その後、一定した値で維持されていることがわかります。
この期間は5年から10年、長い場合、20年間続きます。この期間において明らかな病状は現れませんので,無症状期と呼ばれます。その後、ホストの体調が大きく変化するなどを契機として、HIVウイルスの転写が活発になります。
HIVウイルスの量が増えるに従って、感染細胞であるCD4陽性リンパ球数は急激に減少していきます。免疫反応の中心的な役割を果たしているこの細胞が減少することによって、様々な免疫不全に起因する病状が発症することになります。
29. CD4陽性細胞の減少に伴なう後天性免疫不全症による発症の変化
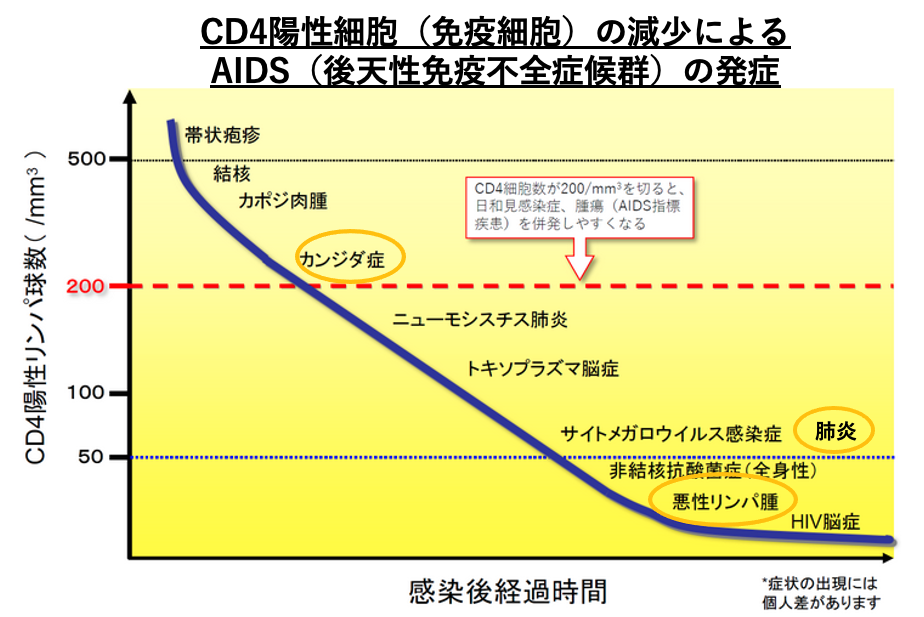
この図では、CD4陽性細胞の減少に伴って生じる。後天性免疫不全症による発症についてまとめています。CD4陽性細胞が、1mLあたり500個ぐらいまで下がりますと、帯状疱疹などが現れます。また、結核などに感染しやすくなります。200前後にまで減少しますと、日和見感染であるカンジダ症にかかりやすくなります。
もっと下がって、50を切ってきますと、肺炎などにかかりやすくなります。50を大きく切りますと、悪性リンパ腫などが発症することになります。このようにHIVウイルスは免疫反応の中心である。CD4陽性細胞に感染し、それを破壊することで、自分自身は免疫反応から逃れて、ホストの細胞内で非常に増えやすい環境を維持しているというふうに考えられます。
30. 宿主細胞由来の癌遺伝子を持つレトロウイルス

ここで少し話題を変えて、宿主細胞由来の癌遺伝子を持つレトロウイルスについて解説をしていきたいと思います。特定のがん組織において,特定のレトロウイルスが発見されることがあります。しかも、そのレトロウイルスは、そのゲノム内に宿主由来のがん遺伝子が埋め込まれている場合があります。
そのような例として、Rouse Sarcoma Virusを取り上げて説明していきます。
31. 細胞破砕濾過液の接種による肉腫の再形成

1911年にRousは、鶏肉腫組織の破砕濾過液を,正常な個体に摂取することで、肉腫を再形成することに成功しました。
まず、鶏の肉腫組織をすりつぶして、セラミックのフィルターでろ過します。その濾過液にはウイルスが含まれています。濾過液をニワトリに摂取することにより、新たに肉腫が形成されたという実験でした。
32. SRC遺伝子を持つRous sarcoma virusのゲノム
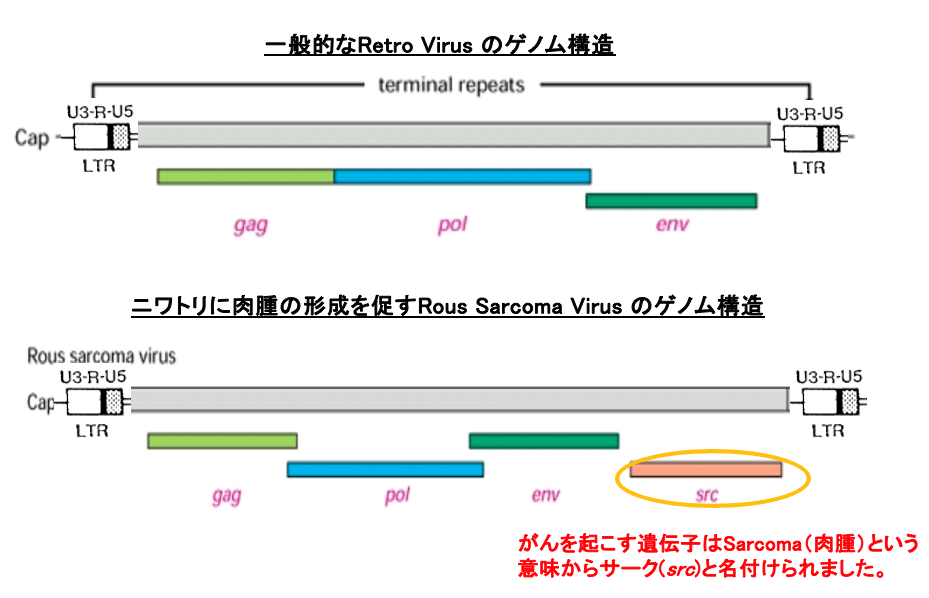
このスライドでは、一般的なレトロウイルスのゲノムと鶏に肉腫を形成させるRous sarcoma virusのゲノム構造を比較しています。一般的なレトロウイルスのゲノム構造は、両末端にlong terminal repeatがあります。遺伝子をコードする大きな領域として、Gag, Pol, Envという三つの領域があります。
一方、Rous sarcoma virusの場合、long terminal repeatが両末端にあって、Gag, Pol, Envという三つのたんぱくコーディング領域があるというのは、上の場合と同じなのですが、Envの下流にsrcという遺伝子が見られます。このsrc geneですが、sarcomaを引き起こす遺伝子という意味で、SRCというふうに名付けられました。
33. 宿主細胞のゲノムにあるSRC遺伝子
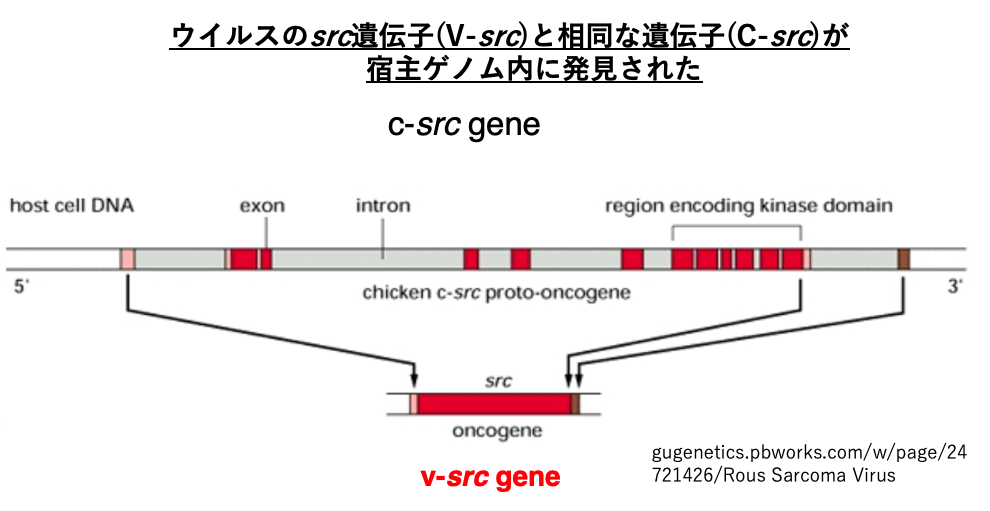
その後の研究により、Rous sarcoma virusのゲノムにあったSRC遺伝子と相同な遺伝子が、宿主細胞のゲノムに発見されました。宿主細胞の中に見つかったサークル遺伝子は、エクソン・イントロンとの構造を持っています。
一方、ウイルスゲノムにあるSRC遺伝子は、この遺伝子がsplicing outされた後の構造をしており、intronは含まれていません。現在では、この二つの遺伝子を区別するために、ウイルス側のSRC遺伝子はV-SRC遺伝子, ゲノム側のサークル選手はC-SRCというふうに記載することになっています。
34. RNA 腫瘍ウイルスが持つ宿主由来ガン遺伝子

その後、同様の研究は続けられ、レトロウイルスについて、多くのがん遺伝子が発見されました。これが先ほどお話したRous sarcoma virusですね。それはSRCと名付けられた遺伝子を持っていたわけですが、今ではこのSRC geneはチロシンカイカイネースをコードしていることがわかっています。
Harvey murine sarcoma virusの場合は、rasをがん遺伝子として持っています。このras遺伝子はGTP binding proteinであるということがわかっています。またAvian myelocytoma virus場合、myc遺伝子を持っています。このmycというのは、転写制御因子の一つです。
このように、レトロウイルスで宿主をがん化させるような能力を持っているウイルスの場合、そのゲノムには、宿主由来であって、細胞の増殖や増殖制御に関わる遺伝子がウイルスゲノム内に含まれているということが次第に明らかになりました。
35. ガン遺伝子をゲノム内に持つレトロウイルスの成立過程
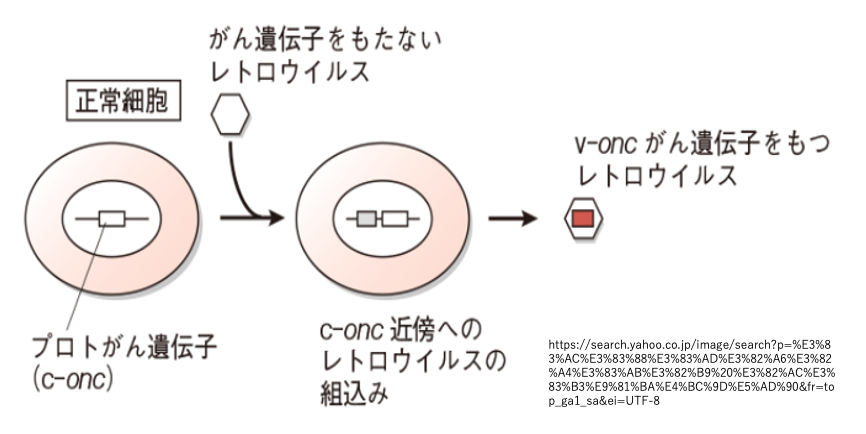
宿主のガン遺伝子をゲノム内に持つレトロウイルスの成立過程について解説をしていきます。今、ここに正常細胞があります。この細胞は、自分自身の細胞増殖のために必要な遺伝子を持っています。そのような細胞増殖に関与する遺伝子がウイルス内に取り込まれますと、がん遺伝子として働きます。
そのため、ウイルス内でガン遺伝子として働く遺伝子は,正常な細胞の中にあるときは、プロトガン遺伝子というふうに呼ばれたりします。その正常細胞に、ガン遺伝子を持たないレトロウイルスが感染します。そのRNAゲノムは、逆転写酵素によってDNA化し、ホストのゲノム内に埋め込まれていきますが、ウイルスのDNAがたまたまプロトガン遺伝子の近辺に埋め込まれたというふうに考えます。
その後、ウイルスは自分自身のDNAを転写してRNAゲノムを生産し、ウイルス粒子を作って、細胞内に出ていくわけですが、そのような過程において、ウイルスゲノムは、oncogene (ガン遺伝子)を自分自身のゲノムの一部として取り込むことで,レトロウイルスが成立したと考えることができます。oncogeneを自分自身のゲーム内に持つようになったレトロウイルスは宿主の細胞をがん化するという能力を得ることによって、自分自身のゲノムを長期にわたり効率よく複製させるように宿主の細胞を変化させている事になります。
36. SRC遺伝子を持つラウス肉腫ウイルス の成立過程
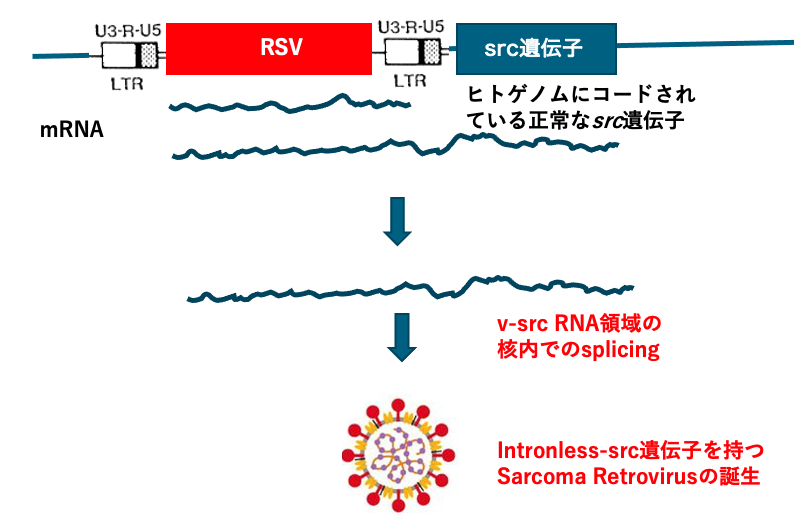
先ほどの仮説について、src遺伝子を持つような、rous sarcoma virusの誕生を例にして説明してみたいと思います。今、rous sarcoma virusが、たまたまホストゲノムのsrc遺伝子の上流に埋め込まれました。通常、この、rous sarcomaの転写は、上流のロングターミナルリピートから始まり、下流のロングターミナルリピートで終わります。
しかし、たまたま転写が下流のロングターミナルリピートで終結せずに、src遺伝子まで続き、src遺伝子の下流で終了したと考えます。そういう長い転写物が作られたとします。この転写物は核内でsplicingを受けます。rous sarcoma virusの遺伝子にはイントロン領域は元々ありませんが、ホーストのsrc遺伝子にはイントロンがたくさんあります。核内でsplicing反応を受けることによって、イントロレスのRNAが出来上がります。
こうして出来上がったイントロレスのsrc遺伝子を持つrous sarcoma virusのRNAゲームがウイルスの殻に埋め込まれることによって、現在私達が見ているようなrous sarcoma virusが成立したというふうに考えることができます。

コメント